
Ensayos clínicos
La unidad de Ensayos Clínicos del IRBLleida pretende consolidar los ensayos clínicos sin interés comercial, potenciar los ensayos clínicos de promotor privado y la búsqueda de la excelencia y el liderazgo en ambos campos.
Objetivos
La unidad tiene como objetivo ofrecer apoyo a los grupos de investigación clínica del Hospital Universitario Arnau de Vilanova y el Hospital Universitario de Santa María de Lleida.
Ámbito de actuación
Quedan incluidos en el ámbito de actuación de la unidad los ensayos clínicos con medicamentos, productos sanitarios y los que estudian otras intervenciones sanitarias terapéuticas. También quedan incluidos los ensayos clínicos aleatorizados de intervención con finalidad diagnóstica, preventiva o de servicio.
Asesoramiento y apoyo
La unidad ofrece asesoramiento y apoyo en aspectos relacionados con métodos y aspectos estadísticos, aspectos regulatorios y de tramitación, aspectos económicos y de gestión de la medicación, ejecución del ensayo, gestión de datos y análisis de los resultados. El asesoramiento y apoyo incluye aspectos que son responsabilidad del promotor y fuerza especializados como los que están relacionados con la documentación, el archivo, la monitorización y el seguimiento de los ensayos clínicos.
Contacto y responsables
Los grupos de investigación clínica se pueden dirigir a la unidad mediante el correo electrónico afernandez(ELIMINAR)@irblleida.cat.
Servicio científico-técnico
Más información en el Servicio científico-técnico Farma y en el documento informativo.
Actividades y servicios
La evaluación ética, metodológica y legal de los ensayos clínicos y proyectos de investigación debe ser realizada por el Comité de Ética de Investigación con Medicamentos (CEI/CEIm) del Hospital Universitario Arnau de Vilanova de la Gerencia Territorial de Lleida y GSS. La legislación española y europea sobre ensayos clínicos requiere un gran desarrollo de las facultades y funciones del Comité de Ética en Investigación Clínica, sobre todo en los ensayos multicéntricos.
Además, el desarrollo de la legislación requiere que los estudios observacionales posteriores a la autorización sean evaluados por el comité. El objetivo principal es contribuir a mejorar la calidad, el manejo y la relevancia de los ensayos clínicos que apuntan a desarrollar nuestro entorno. Esta posición es un claro deseo de fortalecer la posición del Hospital y de su Comité de Ética en Investigación Clínica, no sólo para ser más competitivos en el mercado de la investigación, sino para desarrollar y ejercer liderazgo en la promoción de la investigación de orientación clínica.
Mapa de procesos
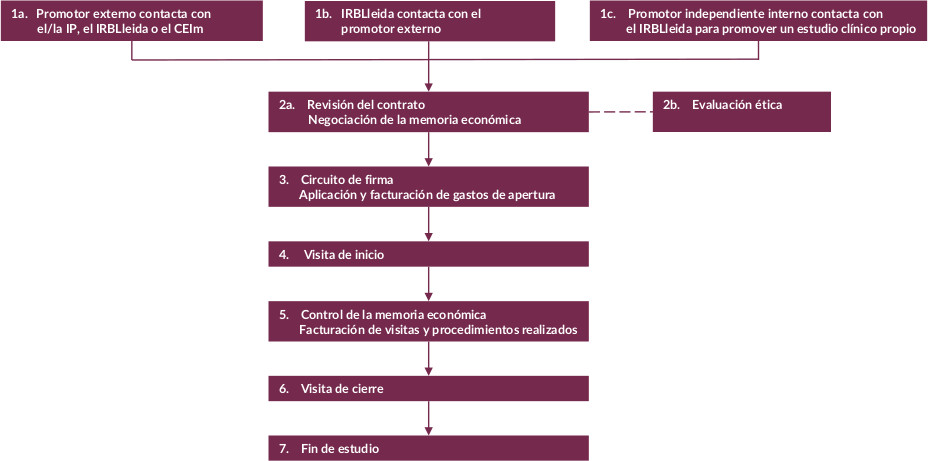
Más información:
- Tarifas (aprobadas por el patronato del IRBLleida el 10/12/2020)
- Tasas CEIm HUAV (CAT)
- Política de overheads






